Амифламин
| Амифламин | |
|---|---|
 | |
| Общие | |
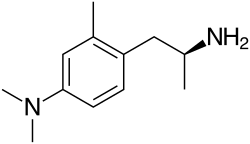
| Систематическое наименование |
4-[(2S)-2-аминопропил]-N,N,3-триметиланилин |
| Сокращения | (+)-4-(диметиламино)-α,2-диметилфенэтиламин |
| Хим. формула | C12H20N2 |
| Физические свойства | |
| Молярная масса | 192.306 г/моль |
| Классификация | |
| Рег. номер CAS | 77518-07-1 |
| PubChem | 71221 |
| SMILES | |
| InChI | |
| ChemSpider | 64356 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Амифламин (FLA-336) является обратимым ингибитором моноаминоксидазы А (МАО-А), таким образом, являясь RIMA, и, в меньшей степени, семикарбазид-чувствительной аминоксидазой (SSAO), а также агентом, высвобождающим серотонин (СВА).[1][2][3][4] Он является производным химических классов фенэтиламина и амфетамина.[1] (+)-энантиомер является активным стереоизомером.[2]
Амифламин ингибирует преимущественно МАО-А в серотонинергических нейронах по сравнению с норадренергическими и дофаминергическими.[5][6] В низких дозировках амифламин функционирует в качестве селективного ингибитора фермента МАО-А в серотониновых клетках, тогда как в более высоких количествах он теряет свою селективность.[5][6] Это свойство объясняется более высокой аффинностью амифламина к транспортёру серотонина по сравнению с транспортёрами норадреналина и дофамина, поскольку для проникновения амифламина в моноаминергические нейроны требуется транспортировка, опосредованная переносчиком.[6]
Смотрите также
- Ингибиторы моноаминоксидазы (MAOI)
Примечания
- 1 2 Anna-Lena Ask, Kerstin Högberg, Lennart Schmidt, Hans Klessling, Svante B. Ross. (+)-4-dimethylamino-2, α-dimethylphenethylamine (FLA 336(+)), a selective inhibitor of the a form of monoamine oxidase in the rat brain // Biochemical Pharmacology. — 1982-04-01. — Т. 31, вып. 7. — С. 1401–1406. — ISSN 0006-2952. — doi:10.1016/0006-2952(82)90035-1. Архивировано 10 июля 2024 года.
- 1 2 Christopher J. Fowler, Märit Eriksson, Gun Thorell, Olle Magnusson. Stereoselective inhibition of monoamine oxidase and semicarbazide-sensitive amine oxidase by 4-dimethylamino-2,α-dimethylphenethylamine (FLA 336) (англ.) // Naunyn-Schmiedeberg's Archives of Pharmacology. — 1984-12-01. — Vol. 327, iss. 4. — P. 279–284. — ISSN 1432-1912. — doi:10.1007/BF00506237. Архивировано 18 февраля 2023 года.
- ↑ Fumio Morikawa, Toshihiko Ueda, Yuichiro Arai, Hiroyasu Kinemuchi. Inhibition of Monoamine Oxidase A-Form and Semicarbazide-Sensitive Amine Oxidase by Selective and Reversible Monoamine Oxidase-A Inhibitors, Amiflamine and FLA 788(+) (англ.) // Pharmacology. — 1986. — Vol. 32, iss. 1. — P. 38–45. — ISSN 1423-0313. — doi:10.1159/000138150.
- ↑ Anna-Lena Ask, Ingrid Fagervall, Ru-Bin Huang, Svante B. Ross. Release of 3H-5-hydroxytryptamine by amiflamine and related phenylalkylamines from rat occipital cortex slices (англ.) // Naunyn-Schmiedeberg's Archives of Pharmacology. — 1989-06-01. — Vol. 339, iss. 6. — P. 684–689. — ISSN 1432-1912. — doi:10.1007/BF00168662. Архивировано 18 февраля 2023 года.
- 1 2 Christopher J. Fowler, Olle Magnusson, Svante B. Ross. Intra- and Extraneuronal Monoamine Oxidase // Blood Vessels. — 2008-09-23. — Т. 21, вып. 3. — С. 126–131. — ISSN 0303-6847. — doi:10.1159/000158505. Архивировано 9 ноября 2024 года.
- 1 2 3 Anna-Lena Ask, Ingrid Fagervall, Svante B. Ross. Selective inhibition of monoamine oxidase in monoaminergic neurons in the rat brain (англ.) // Naunyn-Schmiedeberg's Archives of Pharmacology. — 1983-09-01. — Vol. 324, iss. 2. — P. 79–87. — ISSN 1432-1912. — doi:10.1007/BF00497011. Архивировано 10 ноября 2024 года.