Гексахлороплатинат(IV) аммония
| Гексахлороплатинат(IV) аммония | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Гексахлороплатинат(IV) аммония |
| Традиционные названия | гексахлороплатеат аммония; платиновый нашатырь, нашатырная платина |
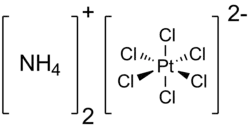
| Хим. формула | (NH4)2[PtCl6] |
| Физические свойства | |
| Состояние | светло-жёлтые кристаллы |
| Молярная масса | 443,88 г/моль |
| Плотность | 3,065 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | разл. 215 °C |
| Энтальпия | |
| • образования | -984,1 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,5020; 2,1680 г/100 мл |
| • в этаноле | 0,005 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,800 |
| Классификация | |
| Рег. номер CAS | 16919-58-7 |
| PubChem | 16211460, 24800213, 57511350 и 13075877 |
| Рег. номер EINECS | 240-973-0 |
| SMILES | |
| InChI | |
| ChEBI | CHEBI:59604 |
| ChemSpider | 10628022 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гексахлороплатинат(IV) аммония — неорганическое соединение, комплексное соединение металла платины с формулой (NH4)2[PtCl6], светло-жёлтые кристаллы, плохо растворяется в воде.
Получение
- Реакция хлорида платины(IV) с концентрированным раствором хлорида аммония:
- Обменная реакция гексахлороплатината(IV) водорода:
Физические свойства
Гексахлороплатинат(IV) аммония образует светло-жёлтые кристаллы кубической сингонии, пространственная группа F m3m, параметры ячейки a = 0,9854 нм.
Плохо растворяется в холодной воде.
Химические свойства
- Разлагается при нагревании:
- Реагирует с разбавленными щелочами:
- Реагирует с концентрированными щелочами:
- С концентрированным раствором аммиака реакция идёт иначе:
- Реагирует с сероводородом:
- Восстанавливается муравьиной кислотой:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.