Гидрофторид натрия
| Гидрофторид натрия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Гидрофторид натрия |
| Традиционные названия | Кислый фтористый натрий; бифторид натрия; гидродифторид натрия |
| Хим. формула | NaHF2 |
| Рац. формула | NaHF2 |
| Физические свойства | |
| Состояние | Бесцветные кристаллы |
| Молярная масса | 61,99 г/моль |
| Плотность | 2,16 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 380 °C |
| • разложения | 270 °C |
| Мол. теплоёмк. | 75 Дж/(моль·К) |
| Энтальпия | |
| • образования | -918 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 3,2520; 7,590 г/100 мл |
| Классификация | |
| Рег. номер CAS | 1333-83-1 |
| PubChem | 219061 и 23446978 |
| Рег. номер EINECS | 215-608-3 |
| SMILES | |
| InChI | |
| ChemSpider | 14213 |
| Безопасность | |
| Предельная концентрация | 1 мг/м³ |
| ЛД50 | 60-140 мг/кг |
| Токсичность | Весьма ядовит |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидрофтори́д на́трия — неорганическое соединение, кислая соль натрия и плавиковой кислоты с формулой NaHF2, бесцветные кристаллы, растворяется в воде. Весьма токсичен.
Получение
- Реакция фторида натрия и плавиковой кислоты:
Физические свойства
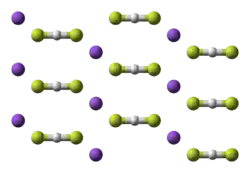
Гидродифторид натрия образует бесцветные кристаллы тригональной сингонии, пространственная группа R 3m, параметры ячейки a = 0,345 нм, c = 1,39 нм, Z = 3.
Умеренно растворяется в воде, не растворяется в органических растворителях. Не образует кристаллогидратов[1].
Химические свойства
- Разлагается при нагревании:
- Разлагается концентрированными щелочами и кислотами[2]:
Сферы использования
- При производстве и обезвоживании плавиковой кислоты.
- Компонент растворов для травления стекла.
- Антисептик.
Стандартизация
В Российской Федерации гидрофторид натрия производился в соответствии с ГОСТ 11037-64[3].
Биологическая роль
- Гидрофторид натрия NaHF2 весьма ядовит (как и другие гидрофториды металлов) в больших количествах.
- Пожаро- и взрывобезопасен.
- ПДК = 1 мг/м³ (по HF).
- ЛД50 на крысах = 149 мг/кг (при пероральном введении).
- Может раздражать слизистые оболочки.
- Вещество принадлежит ко II классу токсичности согласно ГОСТ 12.1.007-76.
Примечания
- ↑ Лидин, 2000, с. 25.
- ↑ Лидин, 2000, с. 26.
- ↑ name=https://docs.cntd.ru Архивная копия от 30 мая 2022 на Wayback Machine
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- CRC Handbook of Chemistry and Physics. — 89th Edition. — Taylor and Francis Group, LLC, 2008—2009.
- Химический энциклопедический словарь / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1983. — 792 с.
- Химические свойства неорганических веществ / под ред. Р.А. Лидина. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
