Гидроортофосфат калия
| Гидроортофосфат калия | |
|---|---|
 | |
| | |
| Общие | |
| Систематическое наименование |
Гидрофосфат калия |
| Традиционные названия | Гидроортофосфат калия, фосфорнокислый калий, двузамещённый |
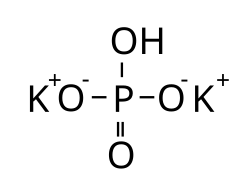
| Хим. формула | K2HPO4 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 174,17 г/моль |
| Плотность | 2,44; гидр. 2,33 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | с разл. 282 °C |
| Мол. теплоёмк. | 141,3 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1775,7 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 159,820; 267,563 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7758-11-4 |
| PubChem | 24450 |
| Рег. номер EINECS | 231-834-5 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E340(ii) |
| ChEBI | 131527 |
| ChemSpider | 22858 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидроортофосфат калия — неорганическое соединение, кислая соль щелочного металла калия и ортофосфорной кислоты с формулой K2HPO4, бесцветные кристаллы, хорошо растворимые в воде, образует кристаллогидраты.
Получение
- Нейтрализация разбавленной ортофосфорной кислоты разбавленным раствором гидроксида или карбоната калия:
- Реакция дигидрофосфата калия с разбавленным раствором гидроксида калия:
Физические свойства
Гидроортофосфат калия образует бесцветные кристаллы ромбической сингонии, пространственная группа P bcm, параметры ячейки a = 1,0314 нм, b = 2,2598 нм, c = 0,5944 нм, Z = 8.
Хорошо растворимы в воде, плохо в этаноле. Водные растворы имеют слабощелочную реакцию из-за гидролиза по аниону.
Образует несколько кристаллогидратов K2HPO4•n H2O, где n = 3 и 6. Гексагидрат при 14,3°С переходит в тригидрат, который при 48,3°С полностью обезвоживается.
Химические свойства
- Кристаллогидрат теряет воду при нагревании:
- При нагревании образует пирофосфат калия:
- С фосфорной кислотой образует дигидрофосфат калия:
- Реагирует с щелочами:
- Вступает в обменные реакции:
Применение
- Для приготовления буферных растворов.
- Как компонент питательной среды для выращивания грибов, производящих пенициллины.
- Фармакология.
- Пищевая добавка Е340.
- Комплексное удобрение.
- Гидрофосфат калия тригидрат относится к многотоннажному химическому производству, цена ≈5$/кг.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
