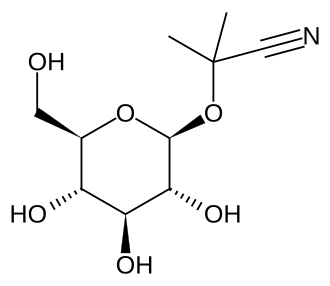
Линамарин
| Линамарин | |
|---|---|
   | |
| Общие | |
| Систематическое наименование |
2-метил-2-[(2S,3R,4S,5S,6R)-3,4,5-тригидрокси-6- (гидроксиметил)оксан-2-ил]окси-пропаненитрил |
| Хим. формула | C10H17NO6 |
| Физические свойства | |
| Состояние | бесцветные иголочки[1] |
| Молярная масса | 247,248 г/моль |
| Плотность | 1,41 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 143–144[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | хорошо растворимо в воде |
| Классификация | |
| Рег. номер CAS | 554-35-8 |
| PubChem | 11128 |
| Рег. номер EINECS | 637-249-5 |
| SMILES | |
| InChI | |
| ChEBI | 16441 |
| ChemSpider | 10657 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Линамарин (англ. Linamarin) — цианогенный гликозид, гликозид циангидрина ацетона, содержащийся в листьях и корнях некоторых растений (маниок, лимская фасоль, лён).
Значение в природе
В природе цианогенные гликозиды защищают растения от травоядных животных. При повреждении тканей растения (во время жевания), линамарин гидролизуются под действием высвобождающегося из клеточных стенок фермента линамаразы из группы β-гликозидаз[2], в результате чего образуются D-глюкоза и ацетонциангидрин, который в свою очередь спонтанно распадается на ацетон и синильную кислоту.
Токсичность
Острое отравление сырыми клубнями маниока характеризуется слабостью, головной болью, тошнотой и рвотой, а в тяжёлых случаях наступает кома и смерть[3]. Летальной дозой для человека являются примерно 400 граммов необработанного горького маниока.
Всосавшийся линамарин быстро выводится с мочой[4].
При длительном употреблении в пищу недостаточно очищенного сырья из маниока происходит хроническое отравление невысокими дозами цианогенных гликозидов (помимо линамарина в растении содержится лотавстралин) и развиваются такие неврологические расстройства, как атаксия, амблиопия и спастическая парестезия, а у детей встречаются неизлечимые виды паралича. В Африке это эндемическое заболевание называют «конзо». Патогенез конзо заключается в нарушении проводимости нервного импульса в спинном мозге (миелопатия).
Показано, что употребление линамарина в пищу может быть фактором риска при развитии невосприимчивости к глюкозе и при диабете, однако, исследования на животных не подтверждают данный факт[5], что может указывать на то, что линамарин лишь усугубляет развитие диабета, но не вызывает его[6].
В результате недавних исследований были получены трансгенные формы маниока, в которых синтез линамарина был стабильно снижен при помощи РНК-интерференции[7].
См. также
Примечания
- 1 2 Shmuel Yannai: Dictionary of Food Compounds with CD-ROM: Additives, Flavors, and Ingredients. CRC Press, 2003, ISBN 9781584884163, P. 695
- ↑ EC 3.2.1.21 // IUBMB Enzyme Nomenclature. Дата обращения: 6 августа 2013. Архивировано из оригинала 15 октября 2012 года.
- ↑ Zuchowski W., 2007, p. 176.
- ↑ Banea-Mayambu JP, Tylleskar T, Gitebo N, Matadi N, Gebre-Medhin M, Rosling H. (1997). Geographical and seasonal association between linamarin and cyanide exposure from cassava and the upper motor neurone disease konzo in former Zaire. Trop Med Int Health 2(12):1143-51. PMID 9438470
- ↑ Soto-Blanco B, Marioka PC, Gorniak SL. (2002). Effects of long-term low-dose cyanide administration to rats. Ecotoxicol Environ Saf 53(1):37-41. PMID 12481854
- ↑ Yessoufou A, Ategbo JM, Girard A, Prost J, Dramane KL, Moutairou K, Hichami A, Khan NA. (2002). Cassava-enriched diet is not diabetogenic rather it aggravates diabetes in rats. Fundam Clin Pharmacol 20(6):579-86. PMID 17109651.
- ↑ Siritunga D, Sayre R (2003). «Generation of cyanogen-free transgenic cassava». Planta 217 (3): 367-73. PMID 14520563