Регорафениб
| Регорафениб | |
|---|---|
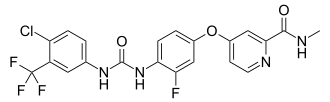 | |
| Химическое соединение | |
| ИЮПАК | 4-[4-({[4-хлоро-3-(трифторометил)фенил]карбамоил}амино)-3-фторофенокси]-N-метилпиридин-2-карбоксамида гидрат |
| Брутто-формула | C21H15ClF4N4O3 |
| Молярная масса | 482,82 г/моль |
| CAS | 755037-03-7 |
| PubChem | 11167602 |
| DrugBank | DB08896 |
| Состав | |
| Классификация | |
| АТХ | L01XE21 |
| Фармакокинетика | |
| Биодоступн. | 69-83% |
| Связывание с белками плазмы | 99.5% |
| Метаболизм | Hepatic (UGT1A9-mediated) |
| Период полувывед. | 20-30 часов |
| Экскреция | Faeces (71%), urine (19%) |
| Способы введения | |
| пероральный | |
| Другие названия | |
| Stivarga | |
Регорафениб (Regorafenib, BAY 73-4506, коммерческое название Stivarga)[1] — пероральный мультикиназный ингибитор, разработанный компанией Bayer, воздействующий на процессы онкогенеза и ангиогенеза в опухолевой ткани, а также нарушающий регуляцию микроокружения опухоли путём ингибирования различных протеинкиназ[2]. В доклинических исследованиях было показано, что Стиварга ингибирует ряд ангиогенных киназ рецепторов VEGF, участвующих в опухолевом неоангиогенезе (формировании новых кровеносных сосудов). С 2018 года включен в Перечень ЖНВЛП.
Примечания
- ↑ Препарат Стиварга (регорафениб) одобрен в ЕС для лечения стромальных опухолей желудочно-кишечного тракта. пресс-релиз компании Вауеr (30 июля 2014). Дата обращения: 30 июля 2014. Архивировано из оригинала 3 августа 2014 года.
- ↑ Регорафениб (Regorafenibum) описание New. rlsnet.ru/. Дата обращения: 11 февраля 2024. Архивировано 1 июля 2023 года.
Ссылки
- Статьи о препарате в базе биомедицинских публикаций PubMed.
| Регорафениб | |
|---|---|
 | |
| Химическое соединение | |
| Брутто-формула | C21H15ClF4N4O3 |
| CAS | 755037-03-7 |
| PubChem | 11167602 |
| DrugBank | DB08896 |
| Состав | |
| Классификация | |
| АТХ | L01XE21 |