Силицид кальция
| Силицид кальция | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Силицид кальция |
| Традиционные названия | Кремнистый кальций |
| Хим. формула | СaSi2 |
| Рац. формула | CaSi2 |
| Физические свойства | |
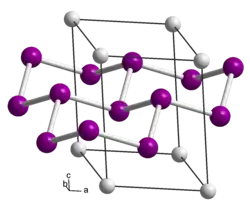
| Состояние | Свинцово-серые блестящие кристаллы |
| Молярная масса | 96,25 г/моль |
| Плотность | 2,5; 2,46 г/см³ |
| Твёрдость | 3 (Шкала Мооса) |
| Термические свойства | |
| Температура | |
| • плавления | 1020; 1033 °C |
| Классификация | |
| Рег. номер CAS | 12013-56-8 |
| PubChem | 13848147 |
| Рег. номер EINECS | 234-588-7 |
| SMILES | |
| InChI | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Силицид кальция — бинарное неорганическое соединение кальция и кремния с формулой СaSi2, свинцово-серые блестящие кристаллы. Впервые получены Вёлером в 1863 году.
Получение
- Непосредственно из элементов (в инертной атмосфере):
- или восстановление оксида кальция кремнием:
Физические свойства
Силицид кальция образует свинцово-серые блестящие кристаллы, тригональной сингонии, пространственная группа R 3m, a = 1,04 нм, α = 21,5°, Z = 2.
Химические свойства
- Разлагается горячей водой:
- Реагирует с минеральными кислотами. Например при взаимодействии с соляной кислотой получается силоксен.
- Горит и может самовоспламеняться на воздухе.
Применение
- В производстве специальных сплавов, для удаления из них фосфора.
- В пиротехнике, в качестве топлива и для производства дыма.
- Специальные термиты (оксиды железа и силицид кальция) — горят без выделения газообразных продуктов.
См. также
Известны другие силициды кальция:
- СaSi — моносилицид кальция
- Сa3Si4
- Сa2Si — двукальциевый силицид
Литература
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.