Соль Фреми
| Соль Фреми | |
|---|---|
 | |
 | |
| Общие | |
| Хим. формула | K2NO7S2 |
| Рац. формула | ON(SO3K)2 |
| Внешний вид | Жёлтые или оранжевые кристаллы |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 268,33 г/моль |
| Термические свойства | |
| Температура | |
| • разложения | >65°С |
| Классификация | |
| Рег. номер CAS | 14293-70-0 |
| PubChem | 3032624 |
| Рег. номер EINECS | 238-219-0 |
| SMILES | |
| InChI | |
| ChEBI | 184372 |
| ChemSpider | 2297553 |
| Безопасность | |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
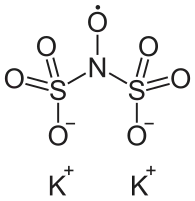
Соль Фреми (нитрозодисульфонат калия) - неорганическое соединение, жёлтые иглообразные кристаллы, водные растворы имеют фиолетовый цвет. Соль примечательна тем, что является свободным радикалом, существующим продолжительное время и использующимся в химической промышленности. В растворе формула вещества ON(SO3K)2, в твердом виде представляет собой димер.
История
Соль Фреми была открыта в 1845 году Эдмоном Фреми. Её открытие под старым названием «сульфазидат калия» засвидетельствовано в французском журнале «L'institut» 23 июля 1845 года[1].
Её использование в органическом синтезе было популяризировано Гансом Тойбером в 1970-х годах. Отсюда окисление с использованием этой соли называется реакцией Тойбера[2][3].
Получение
Нитрозодисульфонат калия получают путем синтеза соли гидроксиламиндисульфоновой кислоты и её окисления. Принцип синтеза можно выразить следующими реакциями:
Практическая составляющая включает множество этапов. Для начала холодный водный раствор нитрита натрия и гидросульфита натрия смешивают с уксусной кислотой(она нужна для вытеснения азотистой кислоты из нитрита), при этом образуется соответствующий гидроксиламин N, N -дисульфонат натрия.
В аммиачной среде он окисляется перманганатом калия до нитрозодисульфоната натрия.
Полученный раствор фильтруют от выпавшего диоксида марганца. К нему приливают раствор хлорида калия(как инертный источник ионов калия).
Потом следует охлаждение раствора и выпадение соли Фреми в осадок из-за её карайне низкой растворимости в холодной воде. Далее раствор вновь фильтруют от примесей и получают соль Фреми в виде оранжево-жёлтых кристаллов.
Соль Фреми следует использовать сразу после получения или поместить под вакуум.
Физические свойства
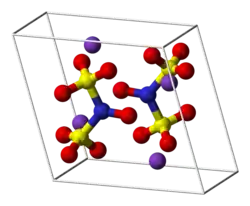
Представляет собой жёлтые или оранжевые кристаллы. Водные растворы имеют фиолетовый цвет. Растворим в воде и этиловом спирте.
Соль Фреми легко разлагается. В чистом виде вещество разлагается примерно в течение суток, в вакууме сохраняется в течение неограниченного времени.
Химические свойства и применение
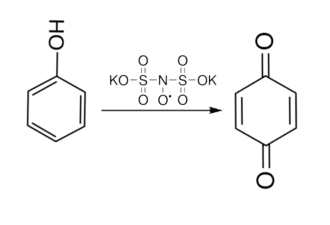
Применение соли Фреми основано на его окислительных свойствах. Это вещество является важным реагентом в органическом синтезе. В частности оно применяется в получении хинонов из фенолов. Реакции использующие нитрозодисульфонат калия для получения хинонов называют реакциями Тойбера[3].
Например окисление фенола и гидрохинона при помощи соли Фреми приводит к образованию 1,4-бензохинона[3].
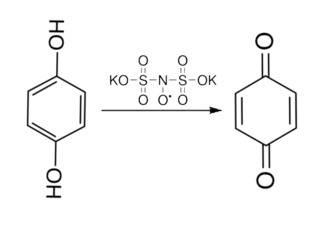
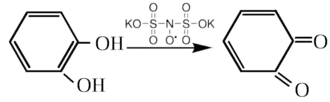
Пирокатехил окисляется до орто-бензохинона[3].
Литература
- Руководство по препаративной неорганической химии под ред. Г. Брауэра, перевод с немецкого. М. 1956.
Примечания
- ↑ L'institut. Section 1: Sciences mathématiques, physiques et naturelles (фр.). — Imprimerie nationale, 1845. — Vol. 13. — P. 265-266. — 514 p.
- ↑ Organic Syntheses Procedure (англ.). orgsyn.org. Дата обращения: 27 мая 2025.
- 1 2 3 4 А.В.Чепраков. Фенолы и хиноны: методы и задачи | Органическая химия. http://orgchem.avchem.ru. Дата обращения: 27 мая 2025.