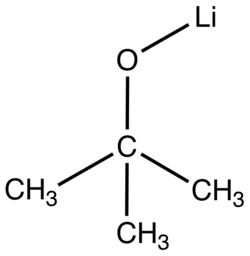
Трет-Бутилат лития
| трет-Бутилат лития[1][2] | |
|---|---|
 | |
| Общие | |
| Хим. формула | C4H9LiO |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 80,07 г/моль |
| Термические свойства | |
| Температура | |
| • сублимации | >170–205 °C |
| • разложения | >250 °C |
| Классификация | |
| Рег. номер CAS | 1907-33-1 |
| PubChem | 24864902 |
| Рег. номер EINECS | 217-611-5 |
| SMILES | |
| InChI | |
| Безопасность | |
| Краткие характер. опасности (H) |
H251, H302, H314 |
| Меры предостор. (P) |
P235, P260, P280, P301+P330+P331, P303+P361+P353, P305+P351+P338 |
| Сигнальное слово | Опасно |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
трет-Бутилат лития — органическое вещество, литиевый алкоголят трет-бутилового спирта. В органическом синтезе находит применение как слабое основание и нуклеофильный алкоголят, например в синтезе трет-бутиловых эфиров и катализе реакций конденсации.
Получение
трет-Бутилат лития коммерчески доступен. В лабораторных условиях его можно приготовить по реакции трет-бутилового спирта с небольшим избытком лития в толуоле при комнатной температуре. Избыток металла после реакции удаляют фильтрованием, а растворитель отгоняют в вакууме. Твёрдый остаток подвергают сублимации. Генерирование трет-бутилата лития in situ достигается введением в реакцию безводного трет-бутилового спирта с н-бутиллитием. Данная реакция экзотермическая, поэтому её поддерживают при комнатной температуре при помощи водяной бани[1].
Применение
Синтез трет-бутиловых эфиров
трет-Бутилат лития позволяет с высоким выходом получать трет-бутиловые эфиры затруднённых карбоновых кислот при реакции с их хлорангидридами. Данный метод подходит также для тех случаев, когда обычный подход с использованием трет-бутилового спирта в присутствии третичного амина не даёт результатов[1].
Реакции конденсации
трет-Бутилат лития служит основным катализатором в реакции присоединения по Михаэлю при условии наличия диполярных апротонных добавок, таких как гексаметилфосфортриамид или 12-краун-4, которые уменьшают степень его агрегации. Подобные результаты получаются и в присутствии трет-бутилата калия[1].
Присоединение к затруднённым кетонам
Известно, что при взаимодействии затруднённых реактивов Гриньяра и разветвлёнными кетонами вместо реакции присоединения происходит реакция восстановления карбонильной группы. Оказалось, что добавка трет-бутилата лития позволяет успешно присоединять диизопропилмагний к ди-трет-бутилкетону, получая выход 81-84 %. Без добавки образуется 88 % продукта восстановления. Точная причина этого явления и роль добавки не выяснены[1].
Примечания
- 1 2 3 4 5 EROS, 2012.
- ↑ Lithium tert-butoxide (англ.). Sigma-Aldrich. Дата обращения: 7 января 2021.
Литература
- Caine D., Roman D. S. Lithium t-Butoxide (англ.) // Encyclopedia of Reagents for Organic Synthesis. — Wiley, 2012. — doi:10.1002/047084289x.rl063.pub2.
Ссылки
- ИК-спектр трет-бутилата лития. Sigma-Aldrich. Дата обращения: 29 июля 2019.