Хинная кислота
| Хинная кислота[1] | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
1,3,4,5-Тетрагидроксициклогексан-карбоновая кислота |
| Хим. формула | C7H12O6 |
| Рац. формула | C7H12O6 |
| Физические свойства | |
| Молярная масса | 192,17 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 166—168 °C |
| Химические свойства | |
| Константа диссоциации кислоты | 3,40 |
| Растворимость | |
| • в воде | 40 г/100 мл |
| Вращение | −43,9° |
| Классификация | |
| Рег. номер CAS | 77-95-2 |
| PubChem | 6508 |
| Рег. номер EINECS | 201-072-8 |
| SMILES | |
| InChI | |
| RTECS | GU8650000 |
| ChEBI | 17521 |
| ChemSpider | 10246715 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хинная кислота — одноосновная полигидроксикарбоновая кислота состава C7H12O6. Представляет собой кристаллическое вещество, содержащееся в коре хины, кофейных зёрнах и многих других растениях. Хинную кислоту получают синтетически гидролизом хлорогеновой кислоты.
Биосинтез
Исходными соединениями для биосинтеза хинной кислоты служат фосфоенолпировиноградная кислота и d-эритрозо-4-фосфат, которые под действием фермента образуют 3-дезокси-d-арабино-гепт-2-улозонат-7-фосфат (ДАГФ), после чего происходит отщепление фосфатного остатка и циклизация в 3-дегидрохинную кислоту, из которой затем получается хинная кислота. Данная схема, являющаяся частью шикиматного пути, доказана для микроорганизмов, однако в высших растениях также были обнаружены ферментные системы, предназначенные для осуществления данной схемы[2].
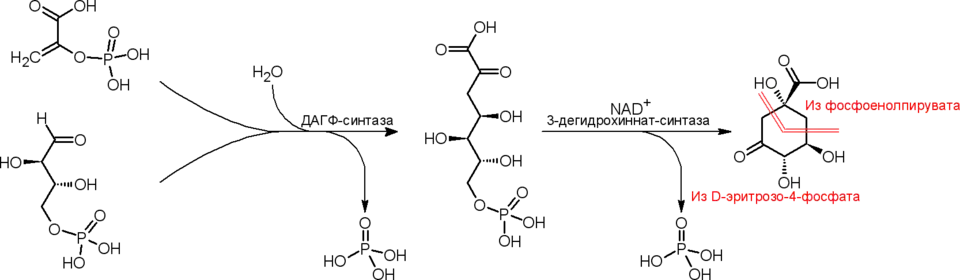
Химические свойства
При нагревании до 200—250 °С хинная кислота превращается в γ-лактон — хинид[3].
Распространение в природе
Хинная кислота была впервые выделена Гофманом в 1790 году из коры хинного дерева. Хинная кислота часто накапливается в растениях в значительных количествах. В частности, из молодых побегов ели удавалось выделить 13,4 % хинной кислоты (в пересчёте на массу сухого сырья)[4]. Также данное соединение обнаружено в табаке, сливах, яблоках, винограде, чернике, клюкве, зёрнах кофе, плодах айвы и др.[2]
Был предложен количественный метод выделения хинной кислоты из фруктов, основанный на относительно высокой растворимости её кальциевой и свинцовой солей по сравнению с солями этих металлов и других органических кислот[5].
Примечания
- ↑ Sigma-Aldrich. D-(−)-Quinic acid. Дата обращения: 4 июля 2013. Архивировано 6 июля 2013 года.
- 1 2 Кретович В. Л. Биохимия растений. — М.: Высшая школа, 1980. — С. 290—292.
- ↑ Досон Р., Эллиот Д., Эллиот У., Джонс К. Справочник биохимика. — М.: Мир, 1991. — С. 52. — 30 000 экз. — ISBN 5-03-001032-7.
- ↑ Запрометов М. Н. Биохимия катехинов: биосинтез, превращения и практическое использование. — М.: Наука, 1964. — С. 150.
- ↑ Kohman E. F., Sanborn N. H. Isolation of Quinic Acid from Fruits (англ.) // Ind. Eng. Chem. — 1931. — Vol. 23, no. 3. — P. 126. — doi:10.1021/ie50254a008.
Ссылки
- ЯМР-спектр хинной кислоты. Дата обращения: 4 июля 2013. Архивировано 6 июля 2013 года.
- ИК-спектр хинной кислоты. Дата обращения: 4 июля 2013. Архивировано 6 июля 2013 года.
- КР-спектр хинной кислоты. Дата обращения: 4 июля 2013. Архивировано 6 июля 2013 года.
