4-Ацетамидо-TEMPO
| 4-Ацетамидо-2,2,6,6-тетраметилпиперидинилоксил[1][2] | |
|---|---|
 | |
| Общие | |
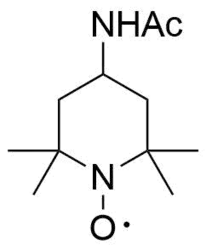
| Систематическое наименование |
4-Ацетамидо-2,2,6,6-тетраметилпиперидинилоксил |
| Традиционные названия | 4-Ацетамидо-TEMPO |
| Хим. формула | C11H21N2O2 |
| Физические свойства | |
| Состояние | красные или розовые кристаллы |
| Молярная масса | 213,30 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 146–147 °C |
| Классификация | |
| Рег. номер CAS | 14691-89-5 |
| PubChem | 518988 |
| Рег. номер EINECS | 423-840-3 |
| SMILES | |
| InChI | |
| ChEBI | 180673 |
| ChemSpider | 452722 |
| Безопасность | |
| Сигнальное слово | Осторожно |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
4-Ацетамидо-2,2,6,6-тетраметилпиперидинилоксил (4-ацетамидо-TEMPO) — органическое вещество, устойчивый свободный радикал. В органическом синтезе используется преимущественно для селективного окисления спиртов.
Получение
В качестве исходного соединения для получения 4-ацетамидо-TEMPO используется 4-амино-2,2,6,6-тетраметилпиперидин[1].
Строение и физические свойства
4-Ацетамидо-TEMPO практически нерастворим в гексане и диэтиловом эфире, растворим в этаноле, ацетоне, ацетонитриле, хлористом метилене, малорастворим в воде. Вещество представляет собой устойчивые, негигроскопичные красные либо розовые кристаллы[1].
Химические свойства
4-Ацетамидо-TEMPO принадлежит к классу нитроксильных радикалов и фактически не используется как самостоятельный окислитель. Вместо этого, под действием пара-толуолсульфокислоты в хлористом метилене его in situ превращают в оксоаммониевую соль, которая сама и является окислителем. В результате реакции образуются лишь необходимое карбонильное соединение и соль гидроксиламина, которая выпадает в осадок. Для выделения продукта смесь необходимо лишь отфильтровать и упарить. Соль гидроксиламина, в свою очередь, можно собрать и количественно превратить в исходный свободный радикал[1].
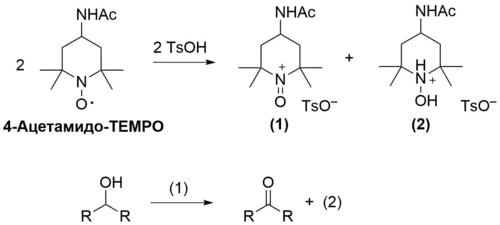
Данный процесс использовали для окисления первичных спиртов и получения соответствующих альдегидов без дальнейшего их окисления. Также этим реагентом можно окислять вторичные спирты с образованием кетонов. Окисление затруднено в тех случаях, когда в β-положении к гидроксильной группе спирта находится атом кислорода или азота. Не вступают в окисление также диолы и углеводы. Реакции мешают амины, тиолы, фенолы, индолы, бензиловые эфиры и кетоны, которые также могут вступать во взаимодействие с реагентом[1].
Примечания
- 1 2 3 4 5 EROS, 2001.
- ↑ 4-Acetamido-TEMPO. Sigma-Aldrich. Дата обращения: 30 июля 2019.
Литература
- Bobbitt J. M., Ma Z. 4-Acetamido-2,2,6,6-tetramethyl-1-piperidinyloxyl (англ.) // Encyclopedia of Reagents for Organic Synthesis. — Wiley, 2001. — doi:10.1002/047084289X.ra006.
Ссылки
- ИК-спектр 4-ацетамидо-TEMPO. Sigma-Aldrich. Дата обращения: 29 июля 2019.