4-Гидроксиазобензол
| 4-Гидроксиазобензол | |
|---|---|
phenol_structure.svg.png) | |
| Общие | |
| Систематическое наименование |
4-(фенилдиазенил)фенол |
| Традиционные названия | 4-гидроксиазобензол, п-фенилазофенол |
| Хим. формула | C6H4OH-N=N-C6H5 |
| Внешний вид | Твёрдое вещество оранжевого или желтоватого цвета |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 198,22 г/моль |
| Плотность | 1,145 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 155 °C |
| • кипения | (при 20 мм рт. ст.) 230 °C |
| Химические свойства | |
| Константа диссоциации кислоты | 8,93 ± 0,13 |
| Растворимость | |
| • в воде | Плохо растворим |
| • в этаноле | Хорошо растворим |
| • в ацетоне | Неограниченно растворим |
| Классификация | |
| Рег. номер CAS | 1689-82-3 |
| PubChem | 15529 |
| Рег. номер EINECS | 216-880-6 |
| SMILES | |
| InChI | |
| ChemSpider | 4510428 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
4-гидроксиазобензол (по ИЮПАК — 4-(фенилдиазенил)фенол) — органическое соединение, получаемое в результате взаимодействия фенола и хлорида фенилдиазония. Оранжевый азокраситель[1].
Получение
Схема образования 4-гидроксиазобензола из фенола и хлорида фенилдиазония (происходит по механизму SE2):[2]
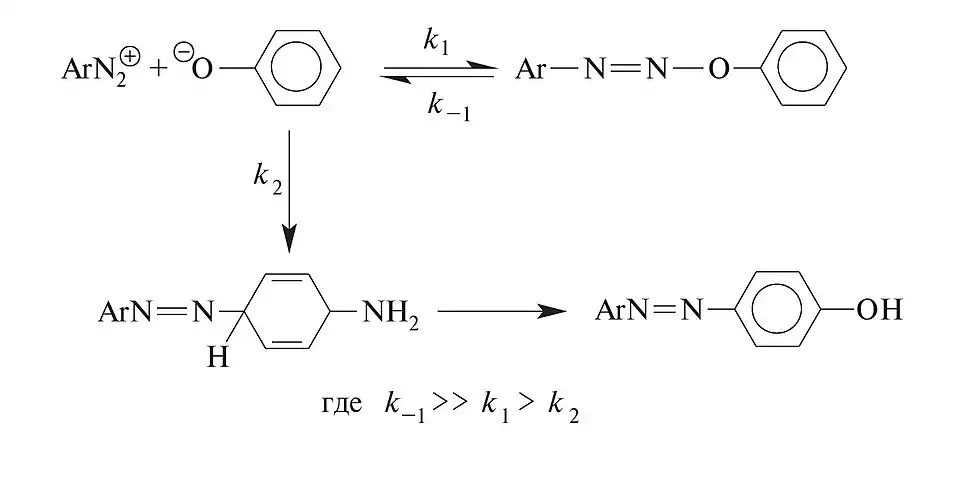
Реакцию проводят в слабощелочной среде (pH 8-10). При этих значениях pH фенол превращается в феноксид-ион, анионный центр которого является одним из самых сильных электронодоноров и соответственно активаторов бензольного кольца по отношению к электрофильной атаке. При более высоких значениях pH соль диазония превращается в диазогидроксид (диазогидрат), который уже не проявляет свойств электрофильной частицы, следовательно, не вступает в реакцию азосочетания. Как видно из представленной схемы, реакция идёт преимущественно по второму пути, т. к. в первом случае скорость обратной реакции во много раз превышает скорость прямой.
Применение
В основном 4-гидроксиазобензол применяют как типичный азокраситель — окрашивание текстиля, биологических тканей, получение других азопроизводных. Ввиду чрезвычайно плохой растворимости в воде, невысокой химической стабильности и относительно высокой токсичности применяется реже, чем другие азокрасители. Сообщается также о применении данного соединения в качестве фунгицида.[3]
Примечания
- ↑ Травень В. Ф. Органическая химия. 1, 2 том. In-chemistry.ru (6 ноября 2014). Дата обращения: 19 мая 2020. Архивировано 14 августа 2020 года.
- ↑ Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия: в 4 ч. Ч. 3 / под ред. канд. хим. наук Т. И. Почкаевой и Г. Г. Есаковой. — 8-е издание. — М.: Лаборатория знаний, 2020. — С. 392. — 547 с. — ISBN 978-5-906828-41-5. — ISBN 978-5-906828-33-0. Архивировано 23 июня 2022 года.
- ↑ 4-PHENYLAZOPHENOL | 1689-82-3 (англ.). ChemicalBook. Дата обращения: 23 июня 2022. Архивировано 25 ноября 2021 года.