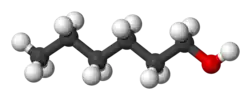
Гексанол
| Гексанол | |||
|---|---|---|---|
| |||
| Общие | |||
| Традиционные названия | 1-гексанол | ||
| Хим. формула | C6H13(OH) | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 102,17 г/моль | ||
| Плотность | 0,82 г/см³ | ||
| Энергия ионизации | 9,89 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -45 °C | ||
| • кипения | 157 °C | ||
| • вспышки | 59 °C | ||
| • самовоспламенения | 293 °C | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 0,59 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 111-27-3 | ||
| PubChem | 8103 | ||
| Рег. номер EINECS | 203-852-3 | ||
| SMILES | |||
| InChI | |||
| RTECS | MQ4025000 | ||
| ChEBI | 87393 | ||
| Номер ООН | 2282 | ||
| ChemSpider | 7812 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Гексанол (1-гексанол, гексиловый спирт) — органическое соединение, относящееся к спиртам. Представляет собой бесцветную горючую жидкость.
Физические свойства
Бесцветная жидкость с приятным запахом. Слабо растворим в воде, хорошо растворим в этаноле и диэтиловом эфире.
Изомеры
Существует два изомера с прямой цепью.
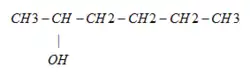
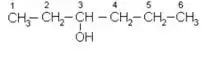
Получение
Промышленный способ получения 1-гексанол, реакция между этиленом и триэтилалюминием с последующим окислением и гидротацией продукта реакции.
Al(C2H5)3 + 6C2H4 → Al(C6H13)3
Al(C6H13)3 +1 1⁄2O2 + 3H2O → 3C6H13OH + Al(OH)3↓
Химические свойства
Гексанол как спирт вступает в реакции этерификации, межмолекулярной дегидратации (получение простых эфиров), окисление спирта приводит к получению гексаналя или гексановой кислоты.
Взаимодействует с щелочными металлами:
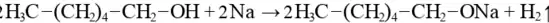
Получение галогеналкана из спирта:
![]()
Нахождение в природе
Является одним из компонентов, отвечающих за аромат клубники.
Присутствует в сигнальном феромоне медоносных пчел.
Применение
Спирт используется:
Примечания
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1-Hexanol | 111-27-3 (англ.). ChemicalBook. Дата обращения: 28 января 2025. Архивировано 28 января 2025 года.
- ↑ ГЕКСАНОЛ (КАПРОНОВЫЙ СПИРТ) (тур.). Ataman Kimya. Дата обращения: 28 января 2025. Архивировано 13 ноября 2024 года.