Дибензо-18-краун-6
| Дибензо-18-краун-6 | |
|---|---|
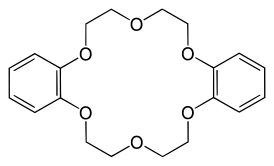 Структура молекулы 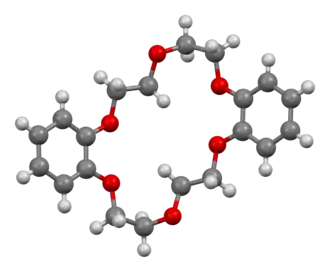 Трёхмерная структура | |
| Общие | |
| Систематическое наименование |
6,7,9,10,17,18,20,21-октагидродибензо[b,k][1,4,7,10,13,16]гексаоксациклооктадецин |
| Традиционные названия | Дибензо-18-краун-6 |
| Хим. формула | C20H24O6 |
| Физические свойства | |
| Состояние | белые волокнистые кристаллы |
| Молярная масса | 360,406 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 162,5-163,5 °C |
| Классификация | |
| Рег. номер CAS | 14187-32-7 |
| PubChem | 26541 |
| Рег. номер EINECS | 238-041-3 |
| SMILES | |
| InChI | |
| RTECS | HP5386000 |
| ChEBI | 358732 |
| ChemSpider | 24722 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дибензо-18-краун-6 — макрогетероцикл из класса краун-эфиров, являющийся первым синтезированным представителем данного класса соединений. Был случайно получен в 1967 году американским химиком Чарльзом Педерсеном[1].
По внешнему виду дибензо-18-краун-6 представляет собой волокнистые белые кристаллы.
Методы получения
Классический и достаточно лёгкий метод получения, по которому изначально и был получен первооткрывателем — реакция пирокатехина с бис(2-хлорэтиловым) эфиром:
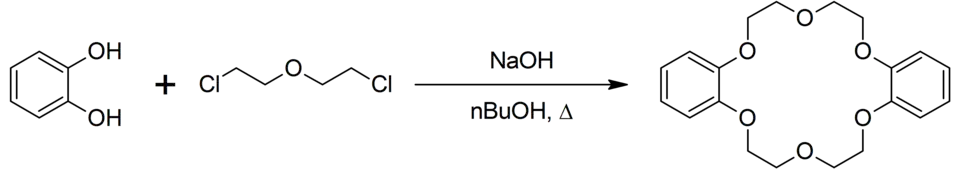
Реакция протекает в достаточно мягких условиях под действием основания (например, гидроксида натрия), которое осуществляет депротонирование OH-групп пирокатехина до фенолят-анионов, выступающих в качестве активных нуклеофильных центров в дальнейшей реакции SN2-замещения с бис(2-хлорэтиловым) эфиром.
Применение
Как и многие другие краун-эфиры, способен образовывать комплексы с катионами металлов (натрия, калия), что делает возможным переведение неорганических солей в неполярные органические растворители и определяет возможность использования этого краун-эфира в качестве межфазного катализатора. Так, известен "пурпурный бензол" — раствор, образующийся при растворении перманганата калия в бензоле в присутствии дибензо-18-крауна-6; этот реагент активно используется в качестве окислителя при проведении реакций в неполярных органических растворителях, например, в реакции окисления толуола до бензойной кислоты.[2]
Примечания
- ↑ MACROCYCLIC POLYETHERS: DIBENZO-18-CROWN-6 POLYETHER AND DICYCLOHEXYL-18-CROWN-6 POLYETHER (англ.) // Organic Syntheses. — 1972. — Vol. 52. — P. 66. — ISSN 2333-3553 0078-6209, 2333-3553. — doi:10.15227/orgsyn.052.0066.
- ↑ Реутов О. А., Бутин К. П, Курц А. Л. Органическая химия. — М.: Лаборатория знаний, 2023. — Т. 3. — С. 176. — 544 с. — ISBN 978-5-00101-336-5.