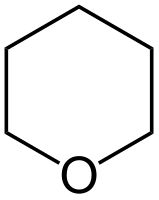
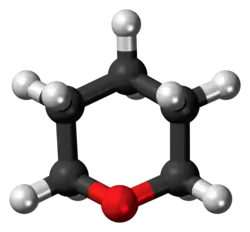
Тетрагидропиран
| Тетрагидропиран | |
|---|---|
  | |
| Общие | |
| Хим. формула | C5H10O |
| Физические свойства | |
| Молярная масса | 86.13 г/моль |
| Плотность | 0.880 г/см³ |
| Энергия ионизации | 9,25 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | −45 °C |
| • кипения | 88 °C |
| Структура | |
| Дипольный момент | 5,8E−30 Кл·м[1] |
| Классификация | |
| Рег. номер CAS | 142-68-7 |
| PubChem | 8894 |
| Рег. номер EINECS | 205-552-8 |
| SMILES | |
| InChI | |
| ChEBI | 46941 |
| ChemSpider | 8554 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тетрагидропиран (пентаметиленоксид, оксан, 1-оксациклогексан) — гетероциклическое органическое соединение с пятью атомами углерода и одним атомом кислорода в цикле (также может рассматриваться как циклический простой эфир).
Методы синтеза
Каталитическое гидрирование дигидропирана (например в присутствии никеля Ренея)[2][3].
Применение
2-Тетрагидропиранильная группа является широко употребляемой защитной группой для спиртов[4]. Ставится она реакцией спиртов с дигидропираном, снимается кислотным гидролизом, образующийся при этом 2-гидрокситетрагидропиран перегруппировывается в 5-гидроксивалериановый альдегид.
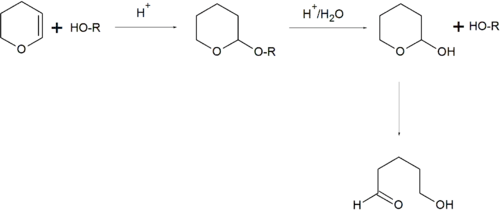
Биологическая роль
Примечания
- 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ D. W. Andrus; John R. Johnson (1955), "Tetrahydropyran", Org. Synth., http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=cv3p0794 Архивная копия от 22 сентября 2008 на Wayback Machine ; Coll. Vol. 3: 794.
- ↑ Синтезы органических препаратов. Сборник 3. — М.: Иностранная Литература, 1952. — с. 403.
- ↑ Дж. МакОми. Защитные группы в органической химии. — М.: Мир, 1976. — с. 104.