Трисульфид дииндия
| Трисульфид дииндия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Трисульфид дииндия |
| Традиционные названия | Сернистый индий |
| Хим. формула | In2S3 |
| Физические свойства | |
| Состояние | тёмно-красные или жёлтые кристаллы |
| Молярная масса | 325,84 г/моль |
| Плотность | 4,648 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1072 °C |
| Энтальпия | |
| • образования | -351 кДж/моль |
| Классификация | |
| Рег. номер CAS | 12030-24-9 |
| PubChem | 16685236 |
| Рег. номер EINECS | 234-742-3 |
| SMILES | |
| InChI | |
| ChemSpider | 17617491 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Трисульфид дииндия — бинарное неорганическое соединение, соль металла индия и сероводородной кислоты с формулой In2S3, тёмно-красные или жёлтые кристаллы, нерастворим в воде, термически устойчив, полупроводник.
Получение
- Непосредственно из элементов:
- Действием сероводорода на его оксид
- Действие сероводорода на растворимую соль индия:
Физические свойства
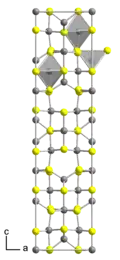
Трисульфид дииндия образует тёмно-красные или жёлтые кристаллы кубической сингонии, параметры ячейки a = 0,536 нм, Z = 1,33. Имеется высокотемпературная кубическая фаза с параметрами ячейки a = 1,0724 нм, Z = 10,667.
Химические свойства
- Реагирует с концентрированными кислотами:
- и концентрированными щелочами:
- При спекании с сульфидом натрия образует тиосоли:
- Окисляется кислородом:
См. также
Существуют другие сульфиды индия:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
