Трифенилфосфин
| Трифенилфосфин | |
|---|---|
 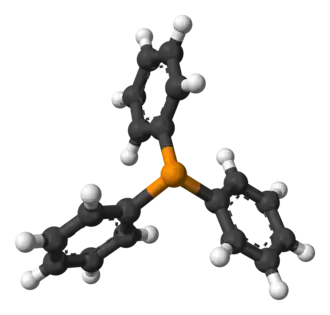 | |
| Общие | |
| Систематическое наименование |
трифенилфосфин |
| Хим. формула | C18H15P |
| Внешний вид | Белые гранулы |
| Физические свойства | |
| Состояние | кристаллическое |
| Молярная масса | 262,29 г/моль |
| Плотность | 1,1 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 80 °C |
| • кипения | 377 °C |
| • вспышки | 182 °C |
| • самовоспламенения | 425 °C |
| Давление пара | 0,017 Па (при 50°C) |
| Химические свойства | |
| Растворимость | |
| • в воде | нерастворим |
| Оптические свойства | |
| Показатель преломления | 1,6358 |
| Структура | |
| Дипольный момент | 1,4 Д |
| Классификация | |
| Рег. номер CAS | 603-35-0 |
| PubChem | 11776 |
| Рег. номер EINECS | 210-036-0 |
| SMILES | |
| InChI | |
| RTECS | SZ3500000 |
| ChEBI | 183318 |
| Номер ООН | 3077 |
| ChemSpider | 11283 |
| Безопасность | |
| Сигнальное слово | Опасно |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Трифенилфосфин — органическое соединение с формулой P(C6H5)3, или просто Ph3P. Является производным фосфина. Имеет вид белых кристаллов. Относительно стабилен при хранении на воздухе. Трифенилфосфин нашёл широкое применение в синтезе металлоорганических соединений. Оксид трифенилфосфина широко используется в микроэлектронике, и по его запаху собак породы лабрадор в США учат находить различные устройства электронной памяти[1].
Получение
В лабораторных условиях трифенилфосфин может быть получен путём взаимодействия трихлорида фосфора с фенилмагнийбромидом или фениллитием. В промышленности трифенилфосфин получают в результате взаимодействия трихлорида фосфора, хлорбензола и натрия
[2].
Физические свойства
Трифенилфосфин – твердое белое вещество без запаха. Обладает триболюминесцентными свойствами. Представляет собой гранулы или крупные кристаллы. Кристаллическая структура напоминает пирамиду. Растворимость в воде 0,09 мг/л при 25 °C, что крайне мало. Хорошо растворим в эфирах; растворим в бензоле , хлороформе, ледяной уксусной кислоте. Плотность 1,1 г/см3.
Химические свойства
Кислородом воздуха трифенилфосфин медленно окисляется с образованием оксида трифенилфосфина:
Трифенилфосфин может быть очищен от примеси оксида путём перекристаллизации из горячего этанола или из горячего изопропанола.[3] Этот метод основывается на том факте, что оксид является более полярным веществом по сравнению с исходным трифенилфосфином, и следовательно, оксид лучше растворим в полярных органических растворителях.
PPh3 является слабым основанием Брёнстеда, однако способен образовывать стабильные соли с сильными кислотами, например с HBr. Компонентом таких солей является катион трифенилфосфония [HPPh3]+.
Cl2 взаимодействует с PPh3 с образованием дихлорида трифенилфосфина ([PPh3Cl]Cl). Это соединение является водочувствительным галогенидом фосфора. В органическом синтезе этот реагент используется для трансформации спиртов в алкилгалогениды.
Применение
Используется как инициатор полимеризации и промежуточное вещество для производства фармацевтических препаратов, солей фосфония и других фосфорных соединений.
Примечания
- ↑ Здесь пахнет электроникой // Наука и жизнь. — 2018. — № 10. — С. 44.
- ↑ D. E. C. Corbridge «Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology» 5th Edition Elsevier: Amsterdam. ISBN 0-444-89307-5.
- ↑ D. D. Perrin, W. L. F. Armarego, D. R. Perrin, Purification of Laboratory Chemicals, 2nd ed.; Pergamon: New York, 1980; p 455.
