1,1,1-трихлорэтан
| 1,1,1-трихлорэтан | |
|---|---|
 | |
| Общие | |
| Традиционные названия | Метилхлороформ, хлоротен |
| Хим. формула | C2H3Cl3 |
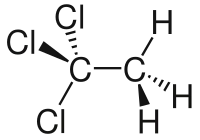
| Рац. формула | CH3CCl3 |
| Внешний вид | Бесцветная жидкость |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 133.404 г/моль |
| Плотность | 1,34 ± 0,01 г/см³[1] |
| Энергия ионизации | 11 ± 1 эВ[1][2] |
| Термические свойства | |
| Температура | |
| • плавления | −23 ± 1 ℉[1] и −30,4 °C[2] |
| • кипения | 165 ± 1 ℉[1] и 74,09 °C[2] |
| Пределы взрываемости | 7,5 ± 0,1 об.%[1] |
| Давление пара | 100 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,048 г/100 мл |
| Структура | |
| Дипольный момент | 5,9E−30 Кл·м[2] |
| Классификация | |
| Рег. номер CAS | 71-55-6 |
| PubChem | 6278 |
| Рег. номер EINECS | 200-756-3 |
| SMILES | |
| InChI | |
| RTECS | KJ2975000 |
| ChEBI | 36015 |
| ChemSpider | 6042 |
| Безопасность | |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
1,1,1-Трихлорэтан, также известный как метилхлороформ — хлоралкан, представляющий собой бесцветную жидкость с душистым запахом. В больших концентрациях ядовит.
История
Впервые трихлорэтан был синтезирован в 1840 году.
Получение
Впервые 1,1,1-трихлорэтан был получен в 1840 году химиком Анри Виктором Ренью. На первом этапе 1,1-дихлорэтан получили по реакции:
Эта реакция катализируется с помощью различных кислот Льюиса, например, хлорида алюминия, хлорида железа (III), или хлорида цинка. Затем 1,1-дихлорэтан превращают в 1,1,1-трихлорэтан по реакции с хлором под ультрафиолетовым облучением:
Выход такого радикального хлорирования составляет 80—90%, а побочный хлористый водород может быть рециркулирован в первый шаг в этом процессе. Основной побочный продукт является изомерным соединением 1,1,2-трихлорэтаном, от которого 1,1,1-трихлорэтан может быть отделен перегонкой.
Несколько меньшее количество 1,1,1-трихлорэтана получают из реакции винилиденхлорида и хлористого водорода в присутствии катализатора — хлорида железа(III)
Химические свойства
1,1,1-трихлорэтан реагирует с растворами щелочей. В реакции со спиртовым расствором образуется хлорацетилен, хлорид щелочного металла и вода:
В реакции с водным раствором образуется ацетат щелочного металла, хлорид щелочного металла и вода:
Безопасность
Малоопасное по степени воздействия на человеческий организм, токсичное вещество[4].
Класс опасности IV по ГОСТ 12.1.005-76[5]. Рекомендуемая ПДК 1,1,1-трихлорэтана в воздухе рабочей зоне составляет 20 мг/м³[6].
Вещество может оказывать негативное воздействие на озоновый слой.
Примечания
- 1 2 3 4 5 6 http://www.cdc.gov/niosh/npg/npgd0404.html
- 1 2 3 4 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1,1,1-трихлорэтан, структурная формула, химические свойства. acetyl.ru. Дата обращения: 15 июня 2025.
- ↑ name=https://docs.cntd.ru_ГОСТ(недоступная+ссылка) 12.1.007-76 система стандартов безопасности труда (ССБТ). Классификация и общие требования безопасности
- ↑ name=https://docs.cntd.ru_ГОСТ(недоступная+ссылка) 12.1.005-76 Система стандартов безопасности труда (ССБТ). Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ↑ name=https://docs.cntd.ru_ГОСТ(недоступная+ссылка) 12.1.005-88 Система стандартов безопасности труда (ССБТ). Общие санитарно-гигиенические требования к воздуху рабочей зоны (с Изменением N 1)
