Тиоцианат ртути(II)
| Тиоцианат ртути(II) | |
|---|---|
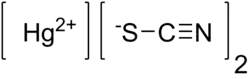 | |
 | |
| Общие | |
| Хим. формула | C2HgN2S2 |
| Классификация | |
| Рег. номер CAS | 592-85-8 |
| PubChem | 11615, 16685035 и 521871 |
| Рег. номер EINECS | 209-773-0 |
| SMILES | |
| InChI | |
| ChemSpider | 11126 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тиоцианат ртути (II) (химическая формула — Hg(NCS)2), также роданид ртути(II) — белый порошок без запаха[1].
Получение и свойства
Получают его обменными реакциями растворов солей тиоциановой кислоты с солями ртути:
При указанной реакции в раствор нитрата ртути необходимо добавить азотной кислоты для предотвращения гидролиза.
Может образовывать комплексные тиоцианаты, например K2[Hg(NCS)4][2].
Может образовать супрамолекулярные соединения с 3-пиридилкарбальдегидом-никотинилгидразоном с вовлечением межмолекулярных взаимодействий[3].
Токсичность
Соединение в порошке и в парах ядовито. Смертельная доза (ЛД50) — 46 мг/кг. При работе с ним следует избегать попадания на слизистые оболочки, в глаза и кожу. При попадании в организм небольших количеств тиоцианатов в течение длительного времени, последние оказывают тиреостатическое действие. Может развиться зоб и дистрофические процессы в различных органах.
Применение
Применяется в аналитической химии как качественный реагент для определения кобальта, галогенидов, цианидов, сульфидов, тиосульфатов, для спектрофотометрических измерений концентрации хлорангидрида изокапроновой кислоты на производстве. Является комплексообразователем. Используется в неорганическом синтезе. Применяется в фотографии для усиления негатива[4].
Опыт «фараонова змея» так же известный, как «борода фараона»
Тиоцианат ртути(II) при нагревании быстро разлагается. Объём продуктов разложения во много раз превышает объём исходной соли, что лежит в основе эффектного опыта «фараонова змея»[5]. Реакция проходит с образованием чёрного сульфида ртути(II) НgS, жёлтого объёмистого нитрида углерода С3N4 и дисульфида углерода СS2, который на воздухе воспламеняется и сгорает, образуя диоксид углерода СО2 и диоксид серы SO2:
Нитрид углерода вспучивается образующимися газами, захватывая чёрный сульфид ртути(II) и образуя жёлто-чёрную пористую массу. Голубое пламя, из которого выползает «змея», — это пламя горящего сероуглерода СS2.
Примечания
- ↑ Ртуть // Энциклопедия Кольера. — Открытое общество. — 2000.
- ↑ Jascha Bandemehr, Matthias Conrad and Florian Kraus. Redetermination of the crystal structure of K2Hg(SCN)4 (англ.) // Acta Crystallographica Section E : Журнал. — 2017. — July (vol. 73, no. 7). — P. 1073-1075. — ISSN 2056-9890. Архивировано 23 февраля 2023 года.
- ↑ Juan D. Velásquez и др. Non-covalent interactions induced supramolecular architecture of Hg(NCS)2 with 3-pyridinecarbaldehyde nicotinoylhydrazone (англ.) // Inorganica Chimica Acta : журнал. — 2020. — 1 September (vol. 509, no. 1). — P. 119700. Архивировано 25 февраля 2023 года.
- ↑ Трахтенберг Т. М., Коршун М. Н. Ртуть и её соединения в окружающей среде. — К.: 1990.
- ↑ LiveLeak.com — Burning Mercury Thiocyanide Will Amaze You. Дата обращения: 30 августа 2011. Архивировано 31 марта 2014 года.
