Типранавир
| Типранавир | |
|---|---|
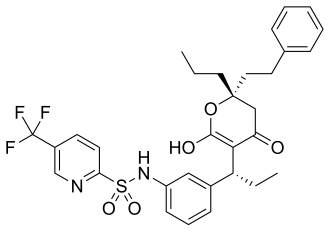 | |
| Химическое соединение | |
| ИЮПАК | N-{3-[(1R)-1-[(2R)-6-hydroxy-4-oxo-2-(2-phenylethyl)-2-propyl-3,4-dihydro-2H-pyran-5-yl]propyl]phenyl}-5-(trifluoromethyl)pyridine-2-sulfonamide |
| Брутто-формула | C31H33F3N2O5S |
| CAS | 174484-41-4 |
| PubChem | 54682461 |
| DrugBank | DB00932 |
| Состав | |
| Классификация | |
| АТХ | J05AE09 |
| Фармакокинетика | |
| Биодоступн. | Не известна |
| Связывание с белками плазмы | >99.9% |
| Метаболизм | Печень (CYP3A4) |
| Период полувывед. | В среднем у мужчин - 5.5 ч - у женщин, 6 ч - у мужчин. |
| Экскреция | Кишечником (82.3%), почками (4.4%) (при приеме с ритонавиром в дозе 500/200 мг) |
| Лекарственные формы | |
| капсулы | |
| Способы введения | |
| Перорально | |
| Другие названия | |
| Не зарегистрирован в РФ | |
Типранавир (TPV) — синтетический противовирусный препарат из группы ингибиторов протеазы для приема внутрь. Типранавир разработан компанией Boehringer Ingelheim и выпускается под торговой маркой Aptivus[1]. Применяется совместно с ритонавиром в составе антиретровирусной терапии для лечения ВИЧ-инфекции.
Фармакологические свойства
Типранавир обладает способностью подавлять репликацию вирусов, устойчивых к другим ингибиторам протеазы, и рекомендуется пациентам, устойчивым к другим видам лечения. Устойчивость к самому типранавиру, по-видимому, требует множественных мутаций[2]. Типранавир был одобрен «Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов» (FDA) 22 июня 2005 года и одобрен для использования в педиатрии 24 июня 2008 года[3].
Типранавир следует принимать только в сочетании с ритонавиром и другими антиретровирусными препаратами, и он не одобрен для пациентов, не получавших лечения[1]. Подобно лопинавиру и атазанавиру, он очень мощный и эффективен в терапии спасения пациентов с лекарственной устойчивостью. Однако побочные эффекты типранавира могут быть более серьезными, чем у других антиретровирусных препаратов. Некоторые побочные эффекты включают внутричерепное кровоизлияние, гепатит, печёночная недостаточность, гипергликемию и сахарный диабет. Также было показано, что препарат вызывает повышение общего холестерина и триглицеридов[1].
На этикетке Aptivus есть предупреждение в виде черного ящика относительно гепатотоксичности и внутричерепного кровоизлияния[1].
Примечания
- 1 2 3 4 Aptivus- tipranavir capsule, liquid filled Aptivus- tipranavir solution. DailyMed (26 июня 2020). Дата обращения: 2 декабря 2020. Архивировано 22 октября 2021 года.
- ↑ Doyon L, Tremblay S, Bourgon L, Wardrop E, Cordingley MG (October 2005). Selection and characterization of HIV-1 showing reduced susceptibility to the non-peptidic protease inhibitor tipranavir. Antiviral Research. 68 (1): 27–35. doi:10.1016/j.antiviral.2005.07.003. PMID 16122817.
- ↑ New Aptivus (tipranavir) Oral Solution Approved for Treatment-Experienced Pediatric and Adolescent HIV Patients (Press release). Boehringer Ingelheim. 24 июня 2008. Архивировано 13 августа 2008. Дата обращения: 2 сентября 2008.