Гексакарбонил молибдена
| Гексакарбонил молибдена | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
карбонил молибдена(VI) |
| Хим. формула | Mo(CO)6 |
| Рац. формула | Mo(CO)6 |
| Физические свойства | |
| Состояние | белые кристаллы, порошок |
| Молярная масса | 264 г/моль |
| Плотность | 1,96 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 148 °C |
| • сублимации | 40 °C |
| • кипения | 155-156 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | нерастворим |
| • в остальных веществах | растворим в бензоле, парафине, слаборастворим в эфире |
| Структура | |
| Координационная геометрия | октаэдр |
| Кристаллическая структура | ортогональная |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 13939-06-5 |
| PubChem | 98885 и 2724068 |
| Рег. номер EINECS | 237-713-3 |
| SMILES | |
| InChI | |
| ChEBI | 30508 |
| Номер ООН | 3466 |
| ChemSpider | 89314 |
| Безопасность | |
| Пиктограммы ECB |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гексакарбонил молибдена — химическое соединение, карбонильный комплекс молибден состава Mo(CO)6, бесцветный твердый кристаллический порошок
Физические свойства
Гексакарбонил молибдена представляет собой двулучепреломляющие диамагнитные бесцветные кристаллы ромбической сингонии, пространственная группа P 2nb, параметры ячейки a = 1,123 нм, b = 1,202 нм, c = 0,648 нм, Z = 4.
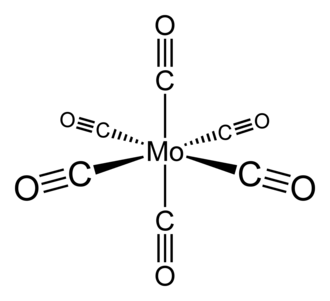
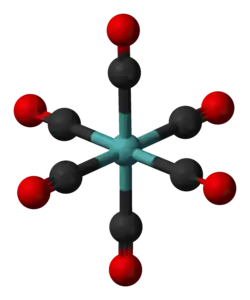
Молекула Mo(CO)6 имеет октаэдрическую геометрию, образованную шестью палочковидных C≡O лигандов, идущих из центрального атома молибдена.
Гексакарбонил молибдена не растворяется в воде и растворах щелочей, реагирует с растворами кислот.
Получение
Гексакарбонил молибдена получают реакцией хлорида молибдена(V) и монооксида углерода под давлением 28 МПа и температуре 200° в присутствии железной стружки.
Нахождение
Mo(CO)6 был обнаружен на свалках и в сточных водах заводов, в анаэробной среде, способствующей формированию Mo(CO)6[1].
Применение
- В органическом синтезе Mo(CO)6 используются в качестве катализаторов. Например, для метатезиса алкинов.
- Нанесение молибденовых покрытий на металлы, керамику, графит.
Безопасность
Как и все карбонилы металлов, Mo(CO)6 является опасным источником летучего металла, также как и CO. Он легко диффундирует в пластиковых сосудах. Может быть смертельным при попадании внутрь организма человека или на кожу[2]
Примечания
- ↑ Feldmann, J. Determination of Ni(CO)4, Fe(CO)5, Mo(CO)6, and W(CO)6 in sewage gas by using cryotrapping gas chromatography inductively coupled plasma mass spectrometry (англ.) // Journal of Environmental Monitoring : journal. — 1999. — Vol. 1. — P. 33—37. — doi:10.1039/a807277i.
- ↑ MSDS for Mo(CO)6 (англ.). Дата обращения: 30 июля 2019. Архивировано 30 июля 2019 года.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
- Химический энциклопедический словарь / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1983. — 792 с.