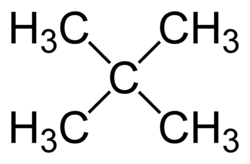
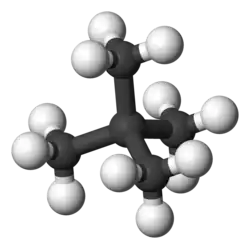
Неопентан
| Неопентан | |
|---|---|
   | |
| Общие | |
| Систематическое наименование |
2,2-диметилпропан |
| Хим. формула | C5H12 |
| Физические свойства | |
| Молярная масса | 72,15 г/моль |
| Плотность | 0,627 г/см³ |
| Энергия ионизации | 10,21 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | −16,6 °C (255 K)[2] |
| • кипения | 9,5 °C (283 K)[2] °C |
| Критическая точка | |
| • температура | 160,75 °C |
| • давление | 3,199 МПа |
| Критическая плотность | 303,5 см³/моль |
| Энтальпия | |
| • образования | −168 кДж/моль |
| • сублимации | −3514 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 3,3⋅10-3 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,342 |
| Структура | |
| Дипольный момент | 0 Кл·м[1] |
| Классификация | |
| Рег. номер CAS | 463-82-1 |
| PubChem | 10041 |
| Рег. номер EINECS | 207-343-7 |
| SMILES | |
| InChI | |
| ChEBI | 30358 |
| ChemSpider | 9646 |
| Безопасность | |
| Фразы риска (R) | R12, R51/53 |
| Фразы безопасности (S) | S9, S16, S33, S61 |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Неопентан (2,2-диметилпропан) — химическое органическое соединение. Химическая формула . Сжижается при температуре ниже 9,5 °C или при высоком давлении. Является одним из трёх структурных изомеров, имеющих молекулярную формулу C5H12 (пентанов); два других — н-пентан и изопентан.
Свойства
Физические свойства
Температура кипения неопентана ниже, чем у изопентана (27,7 °C) и н-пентана (36 °C). Имеет значительно более высокую температуру плавления по сравнению с изопентаном (−16,6 °C против −159,9 °C у изопентана) и н-пентаном (−129,8 °C). Энтропия плавления неопентана почти в 4 раза ниже чем у н-пентана и изопентана[2].
Получение
Может быть получен с помощью реакции Вюрца посредством взаимодействия 2,2-дихлорпропана с метиллитием, диметилцинком (способ М. Д. Львова, при помощи которого неопентан был открыт в 1870[3]) или метилом иодида магния.
Нахождение и применение
Содержится в малых количествах в нефти. Применяется как компонент высококачественного топлива.
Примечания
- 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- 1 2 3 James Wei. Molecular Symmetry, Rotational Entropy, and Elevated Melting Points (англ.). — Ind. Eng. Chem. Res, 1999. — Iss. 12, no. 38. — P. 5019—5027. — doi:10.1021/ie990588m.
- ↑ Zeitschrift für Chemie. — Quandt & Händel, 1870. — 780 с.
Литература
- Петров Ал. А. Химия алканов. — М.: Наука, 1974. — 243 с.
Ссылки
- PubChem — neopentane (англ.). PubChem (16 сентября 2004). Дата обращения: 3 октября 2010. Архивировано 26 мая 2012 года.
- IUPAC Nomenclature of Organic Chemistry (англ.). — Онлайн версия «Голубой Книги» («Blue Book»). Дата обращения: 3 октября 2010. Архивировано из оригинала 21 августа 2011 года.
